Pilihlah salah satu jawaban yang paling tepat!
1. Diketahui unsur X dengan nomor atom 25, maka konfigurasi elektronnya adalah:
A. 1s2 2s2 2p6 3s2 3p6 3d7
B. 1s2 2s2 2p6 3s2 3p3 3d10
C. 1s2 2s2 2p6 3s2 3p6 4s2 3d5
D. 1s2 2s2 2p6 3s2 3p6 4s1 3d6
E. 1s2 2s2 2p6 3s2 3p4 3d9
2. Ion X+ mempunyai konfigurasi elektron 1s2 2s2 2p6. Harga keempat bilangan kuantum elektron valensi dari atom X tersebut adalah……….
A. n = 2, l = 0, m = 0, s = + ½
B. n = 2, l = 0, m = 0, s = - ½
C. n = 3, l = 1, m = 0, s = + ½
D. n = 3, l = 0, m = 0, s = + ½
E. n = 3, l = 0, m = 0, s = – ½
3. Diketahui unsur-unsur: 13 A, 16 B, 18 C, 31 D dan 35 E unsur tersebut yang terletak dalam golongan yang sama adalah…..
A. A dan B
B. B dan C
C. C dan D
D. A dan D
E. A dan E
4. Diketahui suatu atom unsur mempunyai elektron terakhir dengan bilangan kuantum n = 3, l = 2, m = 0 dan s = + ½ maka atom unsur tersebut terletak pada……….
A. Golongan IIIB, periode 5
B. Golongan IIIB, periode 4
C. Golongan VA, periode 4
D. Golongan VB, periode 3
E. Golongan VB, periode 4
5. Diketahui nomor atom Cl = 17 dan F = 9. Dalam molekul ClF3 terdapat..........
A. 7 domain elektron
B. 5 domain elektron
C. 3 domain elektron
D. 2 domain elektron
E. 1 domain elektron
6. Suatu senyawa AB2 dimana nomor atom A = 8 dan B = 9 maka senyawa tersebut mempunyai..........
A. 2 PEI saja
B. 2 PEI dan 1 PEB
C. 2 PEB dan 2 PEI
D. 2 PEI dan 3 PEB
E. 2 PEI dan 4 PEB
7. Diketahui hubungan antara senyawa, tipe molekul dan bentuk molekul
| NO | SENYAWA | TIPE MOLEKUL | BENTUK MOLEKUL |
| 1 | PH3 | AX3 | Piramida trigonal |
| 2 | Cl2O | AX2E2 | Linier |
| 3 | PCl5 | AX5E | Trigonal bipiramida |
| 4 | SF6 | AX6 | Okta hedral |
| 5 | CH4 | AX4 | Segi empat planar |
Dari keterangan yang ada di atas yang sesuai adalah penempatan nomor:
A. 1
B. 2
C. 3
D. 4
E. 5
8. Diketahui nomor atom P = 15, Cl = 17. Jika keduanya membentuk molekul PCl5, maka hibridisasi yang terjadi adalah..........
A. s p2
B. s p3
C. s p3 d2
D. d2 s p3
E. s p3d
9. Diantara pasangan-pasangan senyawa berikut yang keduanya hanya mempunyai gaya dispersi/ gaya London adalah………
A. CO2 dan HCl
B. CH4 dan O2
C. NH3 dan H2S
D. C2H5OH dan CO2
E. CH3COOH dan CH4
10. Berikut ini adalah data titik didih beberapa senyawa hidrida
| Senyawa | HI | HF | HBr | HCl | HCN |
| Titik didih | -35°C | 19,4°C | -67°C | -84°C | -26°C |
Diantara senyawa-senyawa pada data tersebut, yang memiliki ikatan hidrogen paling kuat adalah………..
A. HI
B. HF
C. HBr
D. HCl
E. HI
11. Jika diketahui harga keelektronegatifan H = 2,1 , Br = 2,8, Cl = 3,0, F = 4,0 senyawa-senyawa berikut yang kepolaran nya paling besar adalah.........
A. HCl
B. HBr
C. FCl
D. FBr
E. HF
12. Jika pita magnesium yang panjangnya 2 cm dimasukkan ke dalam tabung reaksi yang berisi 3 cm3 larutan HCl 2M, ternyata terbentuk gelembung gas dan dasar tabung terasa panas. Reaksi ini dapat digolongkan………
A. Endoterm, energi berpindah dari lingkungan ke sistem.
B. Endoterm, energi berpindah dari sistem ke lingkungan
C. Eksoterm, energi berpindah dari lingkungan ke sistem
D. Eksoterm, energi berpindah dari sistem ke lingkungan
E. Eksoterm karena sistem menjadi panas.
13. Pada proses endoterm.......
A. Entalpi sistem bertambah dan perubahan entalpi positif
B. Entalpi sistem bertambah dan perubahan entalpi negatif
C. Entalpi sistem berkurang dan perubahan entalpi positif
D. Entalpi sistem berkurang dan perubahan entalpi negatif
E. Entalpi lingkungan bertambah dan perubahan entalpi negatif.
14. Perhatikan berbagai hasil percobaan berikut!
1. Reaksi kristal NH4Cl dan kristal Ba(OH)2, timbul gas berbau tidak enak dan disertai penurunan suhu.
2. Pita Mg dan larutan HCl , timbul gas dan disertai kenaikkan suhu.
3. Serbuk besi dan serbuk belerang tidak terjadi perubahan, tetapi berubah menjadi zat padat hitam setelah dipanaskan, reaksi berlanjut ketika pemanasan dihentikan.
4. Gas N2O4 yang tidak berwarna berubah menjadi coklat jika dipanaskan, jika pemanasan dihentikan perlahan-lahan, kembali tidak berwarna.
Proses yang tergolong reaksi eksoterm adalah.........
A. 1 dan 3
B. 2 dan 3
C. 2 dan 4
D. 3 dan 4
E. 1 dan 4
15. Pada pembakaran 4 gr gas metana (CH4) dibebaskan 55,6 KJ. (Mr CH4 = 16). Persamaan termokimia yang menggambarkan reaksi pembakaran metana adalah........
A. CH4 (g) + 2O2 (g) ® CO2 (g) + 2H2O (l) ∆H = -55,6 KJ
B. CH4 (g) + 2O2 (g) ® CO2 (g) + 2H2O (l) ∆H = +55,6 KJ
C. CH4 (g) + 2O2 (g) ® CO2 (g) + 2H2O (l) ∆H = - 222,4 KJ
D. CH4 (g) + 2O2 (g) ® CO2 (g) + 2H2O (l) ∆H = + 222,4 KJ
E. CH4 (g) + O2 (g) ® CO2 (g) + H2O (g) ∆H = -55,6 KJ
16. Kalor pembakaran asetilina pada reaksi:
C2H2 (g) + 2½ O2 (g) ® 2CO2 (g) + H2O (l) ∆H = a kkal / mol
∆Hf° CO2 (g) = b kkal / mol dan H2O (l) = c kkal / mol.
Berdasarkan Hukum Hess, entalpi reaksi pembentukan C2H2 adalah………
A. –a + 2b + c
B. –a – 2b + c
C. –a – 2b – c
D. +a – 2b + c
E. +a – 2b – c
17. Diketahui entalpi pembentukan standar beberapa senyawa
∆Hf H2O (l) = -258 KJ mol-1
∆Hf CO2 (g) = -393 KJ mol-1
∆Hf C2H4 (g) = 52,26 KJ mol-1
Pada reaksi C2H4 (g) + O2 (g) ® CO2 (g) + H2O (l) (reaksi belum setara), kalor yang dibebaskan adalah……..
A. -598,74 KJ
B. + 598, 74 KJ
C. – 1249,74 KJ
D. + 1249,74 KJ
E. – 703, 26 KJ
18.
 |
Sesuai dengan diagram tingkat energi disamping, maka pada penguapan 18 gram air dari tubuh mengakibatkan.......
A. Tubuh kehilangan energi 285,5 kJ
B. Tubuh mendapat energi sebanyak 285,5 kJ
C. Tubuh mendapatkan energi 87 kJ
D. Tubuh mendapatkan energi 43,5 kJ
E. Tubuh kehilangan energi sebanyak 43,5 kJ
19. Entalpi pembentukan gas NO = + 90 kJ/mol.
Jika energi ikatan N ≡ N ; 418 kJ.mol-1
O = O ; 498 kJ mol-1
Maka energi yang dibutuhkan untuk memutuskan satu mol ikatan NO adalah....
A. 413 kJ
B. 765 kJ
C. 720 kJ
D. 826 kJ
E. 911 kJ
20. Jika data entalpi beberapa reaksi sebagai berikut:
CS2(l) + 3O2(g) ® CO2(g) + 2SO2 (g) ∆H = -1110 kJ
C(s) + O2(g) ® CO2(g) ∆H = -394 kJ
S(s) + O2(g) ® SO2(g) ∆H = -297 kJ
Maka entalpi pembentukan CS2 adalah…………..
A. -122 kJ
B. + 122 kJ
C. + 419 kJ
D. - 419 kJ
E. + 906 kJ
21. Molaritas larutan KI yang dibuat dengan melarutkan 0,1 mol KI ke dalam air yang volumenya 2 Liter adalah....
A. 0,05 M
B. 0,2 M
C. 0,5 M
D. 2,0 M
E. 2,5 M
22. Larutan asam nitrat kadarnya 63% dan massa jenisnya 1,5 gr/cm3. Jika akan dibuat asam nitrat sebanyak 150 mL dengan konsentrasi 0,5 M (Ar H = 1, N = 14, O = 16), maka asam nitrat pekat di atas yang diperlukan adalah....
A. 2 mL
B. 2,5 mL
C. 3 mL
D. 4,5 mL
E. 5 mL
23. Perhatikan data percobaan untuk reaksi: Zn(s) + 2HCl (aq) → Cl2 (aq) + H2 (g). Berdasarkan percobaan 4 dan 5, laju reaksi dipengaruhi oleh...
| No | Massa Zn | Konsentrasi HCl | Waktu (menit) | Suhu (oC) |
| 1. 2. 3. 4. 5. | 5 gr serbuk 5 gr lempengan 5 gr serbuk 5 gr lempengan 5 gr lempengan | 0,1 M 0,1 M 0,2 M 0,2 M 0,1 M | 3 5 1 2 1,5 | 25 25 25 25 40 |
A. Luas permukaan dan suhu
B. Konsentrasi dan suhu
C. Luas permukaan dan konsentrasi
D. Suhu dan luas permukaan
E. Konsentrasi dan massa zat
24. Kenaikan suhu umumnya menaikkan laju reaksi, alasannya yang tepat adalah...
A. Energi kinetik dari molekul-molekul menurun
B. Kenaikan suhu dapat menghasilkan reaksi setimbang
C. Laju masing-masing molekul menjadi berimbang
D. Energi kinetik dari molekul-molekul meningkat
E. Kenaikan suhu memperkecil energi aktivasi
25. Dari percobaan peruraian H2O2 menjadi H2O dan O2 diperoleh data sebagai berikut.
| Percobaan | Pengamatan |
| 1. Larutan H2O2 saja 2. Larutan H2O2 + Larutan NaCl 3. Larutan H2O2 + Fe2(SO4)3 4. Larutan H2O2 + CoCl2 | Sedikit gelembung Sedikit gelembung Banyak gelembung Banyak gelembung |
Dari data di atas, zat yang berfungsi sebagai katalis dalam peruraian H2O2 adalah..
A. Co2+ dan Fe2+
B. Na+ + Fe2+
C. Co2+ + Fe3+
D. Co3+ + Fe2+
E. Na+ + Co2+
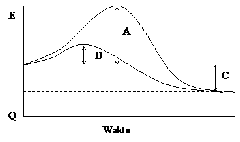
26.
Dari diagram di atas dapat dijelaskan pada reaksi yang menggunakan katalis tentang energi aktivasi
A. A adalah energi aktivasi yang tetap
B. C adalah energi aktivasi yang turun
C. B adalah energi aktivasi yang turun
D. A + B adalah jumlah energi aktivasi
E. B + C adalah jumlah energi aktivasi
27. Dari reaksi 2NO(g) + 2H2(g) → N2(g) + 2H2O(g) diperoleh data sebagai berikut:
| No percobaan | Konsentrasi (mol.L-1) | Laju reaksi (M.s-1) | |
| NO | H2 | ||
| | 2 x 10-2 4 x 10-2 6 x 10-2 4 x 10-2 4 x 10-2 | 2 x 10-2 2 x 10-2 2 x 10-2 6 x 10-2 8 x 10-2 | 4 x 10-3 8 x 10-3 12 x 10-3 24 x 10-3 32 x 10-3 |
Orde reaksi tersebut adalah....
A. 1
B. 2
C. 3
D. 4
E. 5
28. Laju reaksi berubah menjadi 2 kali lebih cepat setiap kenaikan suhu 10 oC. Jika pada suhu 35 oC waktu reaksi adalah 32 detik, maka waktu reaksi pada suhu 25 oC dan 55 oC adalah...
A. 4 dan 128 detik
B. 8 dan 128 detik
C. 64 dan 128 detik
D. 64 dan 8 detik
E. 128 dan 4 detik
29. Berikut merupakan peranan katalis. Peranan katalis yang benar adalah....
A. Katalis V2O5 digunakan dalam industri amoniak
B. Katalis Pt-Ra digunakan dalam industri asam sulfat
C. Katalis enzim sinase digunakan dalam industri MSG
D. Katalis Fe2+ digunakan dalam industri H2O2
E. Katalis logam besi dan aluminium oksida digunakan dalam industi amoniak
30. Reaksi dinyatakan setimbang jika....
A. Laju reaksi ke kanan sama dengan laju reaksi ke kiri
B. Reaksi sudah berhenti
C. Jumlah mol sebelah kanan sama dengan jumlah mol sebelah kiri
D. Semua pereaksi habis bereaksi
E. Diperoleh hasil yang maksimal
31. Diketahui reaksi kesetimbangan: Al3+ (aq) + 3H2O (l) D Al(OH)3 (s) + 3H+ (aq). Harga tetapan kesetimbangan adalah....
32. Dari reaksi kesetimbangan berikut, peningkatan tekanan yang menyebabkan reaksi bergeser ke kanan adalah....
A. N2(g) + 3H2(g) D 2NH3(g)
B. N2O4(g) D 2NO2(g)
C. CaO(s) + CO2(g) D CaCO3(g)
D. CuO(s) + H2(g) D Cu(s) + H2O(g)
E. Fe3O4(g) + 4H2(g) D 3Fe(s) + 4H2O(g)
33. Reaksi antara FeCl3(aq) dengan KCN(aq) membentuk reaksi kesetimbangan sebagai berikut: Fe3+(aq) + SCN-(aq) D [Fe(SCN)]3+(aq).
Jika ditambahkan Na2HPO4 ke dalam sistem tersebut ternyata warna merah berkurang, hal tersebut terjadi karena....
A. Pengurangan semua konsentrasi zat dan harga Kc tetap
B. Konsentrasi SCN- bertambah dan harga Kc tetap
C. Kesetimbangan bergeser ke kanan dan harga Kc tetap
D. Kesetimbangan bergeser ke kiri dan harga Kc makin kecil
E. Konsentrasi ion Fe3+ berkurang dan harga Kc tetap
34. Pembuatan gas SO3 menurut proses kontak sesuai dengan reaksi berikut:
2SO(g) + O2(g) D 2SO3(g) DH = - 44,5 kkal.
Supaya produksi SO3 dapat diperbesar dengan cara...
A. Memperbesar volume
B. Memperkecil volume
C. Menambah katalis V2O5
D. Mengurangi SO2
E. Menurunkan temperatur
35. Perhatikan kesetimbangan berikut:
2NO2(g) D 2NO(g) + O2(g) DH = + 150 kJ
Apabila pada volume tetap, suhu dinaikkan maka kesetimbangan bergeser ke arah...
A. Kanan dan harga K tetap
B. Kiri dan harga K makin kecil
C. Kanan dan harga K makin kecil
D. Kiri dan harga K makin besar
E. Kanan dan harga K makin besar
36. Dalam wadah 5 liter terdapat 4 mol asam iodida, 0,5 mol iod dan 0,5 mol gas hidrogendalam keadaan setimbang. Tetapan kesetimbangan untuk reaksi pembentukan asam iodida dari iodin dan hidrogen adalah...
A. 64
B. 60
C. 54
D. 50
E. 46
37. Dalam suatu bejana yang volumenya 1 L, 4 mol gas NO2 membentuk kesetimbangan sebagai berikut:
2NO2(g) D 2NO(g) + O2(g).
Dalam keadaan setimbang, pada suhu tetap, terbentuk 1 mol gas O2. Nilai tetapan kesetimbangan (Kc) adalah...
A. 0,5
B. 1,0
C. 1,5
D. 2,0
E. 4,0
38. Dalam ruang 5 Liter terdapat kesetimbangan gas PCl5 yang mengalami dissosiasi menghasilkan PCl3 dan Cl2. Jika pada keadaan tersebut mol PCl5, PCl3 dan Cl2 berturut-turut 0,3 mol; 0,2 mol; 0,2 mol, maka derajat dissosiasinya adalah...
A. 0,04
B. 0,2
C. 0,3
D. 0,4
E. 0,5
39. Pada suhu t oC dalam sebuah bejana dengan volume V Liter terdapat kesetimbangan sebagai berikut:
2X(g) D 3Y(g)
Nilai Kp pada suhu tersebut ½ . Jika tekanan parsial X adalah 2 atm, maka tekanan pasial Y pada suhu tersebut adalah...
A. 1,3 atm
B. 1,5 atm
C. 2,0 atm
D. 5,6 atm
E. 8,0 atm
40. Pada industri amoniak menurut Proses Haber Bosch, terjadi reaksi kesetimbangan antara gas N2(g) + 3H2(g) D 2NH3(g) efektif pada suhu 550 oC, dan reaksi tersebut berlangsung eksoterm. Untuk mengoptimalkan produksi NH3 dapat dilakukan dengan beberapa cara, kecuali...
A. Menaikkan tekanan
B. Menurunknan suhu
C. Menambah katalis serbuk besi dan Al2O3
D. Menaikkan suhu
E. Memisahkan hasil reaksi
I. Essay
Jawablah soal-soal berikut dengan singkat dan tepat
41. Tentukan bentuk molekul senyawa CCl4 dan PH3 berdasarkan teori hibridisasi!
( C = 6, Cl = 17, H = 1 P = 15 )
42. Diketahui entalpi pembentukan CO2(g) = -394 kJ/mol, H2O(l) = -286 kJ/mol dan C3H8(g) = -104 kJ/mol Tentukan jumlah kalor yang dapat dibebaskan jika 22 gram C3H8(g) dibakar sempurna membentuk gas CO2 dan air (C=12 , H = 1)
43. Pada volume 4 L dimasukkan 10 mol PCl5 (g) dan dibiarkan terjadi kesetimbangan sesuai dengan persamaan reaksi:
PCl5(g) D PCl3(g) + Cl2(g)
Jika pada keadaan setimbang terdapat 4 mol Cl2 dan pengukuran dilakukan pada suhu 27oC, tentukan: α, Kc dan Kp jika R = 0,082 L.atm.mol-1.K-1












Posting Komentar